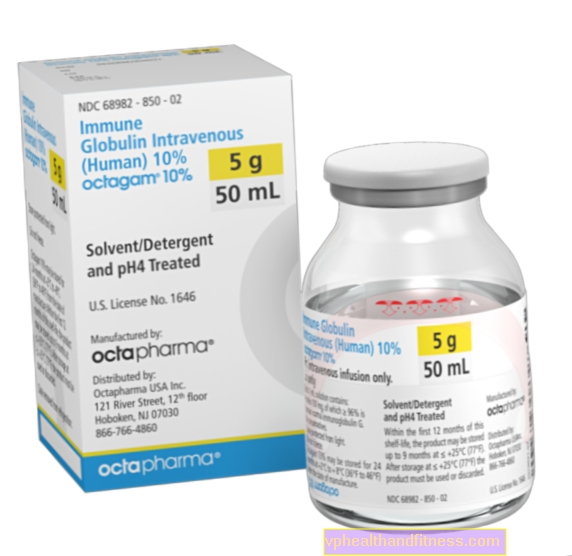
สารละลาย 1 มิลลิลิตรประกอบด้วยอิมมูโนโกลบูลินปกติของมนุษย์ 100 มก. (รวม IgG อย่างน้อย 95%) การกระจายของคลาสย่อย IgG: IgG1 - ประมาณ 60%, IgG2 - ประมาณ 32%, IgG3 - ประมาณ 7%, IgG4 - ประมาณ 1% ปริมาณ IgA สูงสุดไม่เกิน 0.4 มก. pH ของสารละลายคือ 4.5 - 5.0; osmolality คือ≥ 240 mOsmol / kg ยานี้มีโซเดียมไม่เกิน 0.03 mmol (0.69 mg) ต่อมิลลิลิตรของสารละลาย การเตรียมประกอบด้วยมอลโตส
| ชื่อ | เนื้อหาของแพ็คเกจ | สารออกฤทธิ์ | ราคา 100% | แก้ไขล่าสุด |
| Octagam 10% | รองเท้า. 200 มล. โซล. ถึง inf. | อิมมูโนโกลบูลินของมนุษย์ปกติ | 2019-04-05 |
หนังบู๊
อิมมูโนโกลบูลินปกติของมนุษย์ส่วนใหญ่ประกอบด้วยอิมมูโนโกลบูลิน G (IgG) ที่ไม่เปลี่ยนแปลงตามหน้าที่โดยมีแอนติบอดีต่อสารติดเชื้อในวงกว้าง มันมีการกระจายของคลาสย่อยอิมมูโนโกลบูลิน G ตามสัดส่วนที่ใกล้เคียงกับในพลาสมาของมนุษย์ ปริมาณอิมมูโนโกลบูลินปกติของมนุษย์ในปริมาณที่สูงเพียงพอสามารถทำให้ระดับอิมมูโนโกลบูลิน G ที่ต่ำผิดปกติกลับเข้าสู่ช่วงปกติได้ กลไกการออกฤทธิ์ของยาที่ใช้กับข้อบ่งชี้อื่น ๆ นอกเหนือจากการบำบัดทดแทนนั้นไม่ได้รับการอธิบายอย่างเต็มที่ แต่เป็นที่ทราบกันดีว่าเกี่ยวข้องกับผลของภูมิคุ้มกัน อิมมูโนโกลบูลินปกติของมนุษย์สามารถดูดซึมได้ทันทีและสมบูรณ์ในการไหลเวียนของผู้รับหลังการให้ทางหลอดเลือดดำ มีการกระจายค่อนข้างเร็วระหว่างพลาสมาและของเหลวนอกเซลล์ หลังจาก 3-5 วันจะมีการสร้างสภาวะสมดุลระหว่างช่องภายในและช่องพิเศษของหลอดเลือด ครึ่งชีวิตของ IgG ในผู้ป่วยที่มีภูมิคุ้มกันต่ำหลังการให้ยาอยู่ระหว่าง 26 ถึง 41 วัน ครึ่งชีวิตอาจแตกต่างกันไปในแต่ละผู้ป่วยโดยเฉพาะอย่างยิ่งในกรณีของภาวะภูมิคุ้มกันบกพร่องขั้นต้น อิมมูโนโกลบูลินจี (IgG) และสารประกอบเชิงซ้อนจะถูกย่อยสลายในเซลล์ของระบบเรติคูโลเอนโดทีเลียล
ปริมาณ
ฉีดเข้าเส้นเลือด ผู้ใหญ่และเด็ก (0-18 ปี) ควรเริ่มต้นและติดตามการบำบัดทดแทนภายใต้การดูแลของแพทย์ที่มีประสบการณ์ในการรักษาภาวะภูมิคุ้มกันบกพร่อง ขนาดยาและวิธีการใช้ยาขึ้นอยู่กับข้อบ่งชี้ ในการบำบัดทดแทนอาจจำเป็นต้องปรับขนาดยาเป็นรายบุคคลสำหรับผู้ป่วยทั้งนี้ขึ้นอยู่กับการตอบสนองทางเภสัชจลนศาสตร์และทางคลินิก ตารางการให้ยาต่อไปนี้เป็นแนวทาง การบำบัดทดแทนในภาวะภูมิคุ้มกันบกพร่องเบื้องต้น ระบบการให้ยาควรได้ระดับ IgG trough (วัดก่อนการให้ยาครั้งต่อไป) อย่างน้อย 5-6 g / l ใช้เวลา 3-6 เดือนนับจากเริ่มการรักษาเพื่อแก้ไขการขาดแอนติบอดี ปริมาณเริ่มต้นที่แนะนำคือ 0.4-0.8 กรัม / กก. บริหารครั้งเดียวจากนั้นใช้น้ำหนักตัว 0.2 กรัม / กก. ทุกๆ 3-4 สัปดาห์ต้องใช้ยา 0.2-0.8 g / kg bw / เดือนเพื่อให้ได้ระดับ IgG ที่ 5-6 g / l ช่วงเวลาระหว่างปริมาณหลังจากเข้าสู่สภาวะคงที่คือ 3-4 สัปดาห์การกำหนดและประเมินความเข้มข้นของรางน้ำควรทำโดยสัมพันธ์กับอุบัติการณ์ของการติดเชื้อ อาจจำเป็นต้องเพิ่มขนาดยาและมุ่งเป้าไปที่ระดับรางที่สูงขึ้นเพื่อลดอัตราการติดเชื้อ Hypogammaglobulinaemia และการติดเชื้อแบคทีเรียซ้ำในผู้ป่วยมะเร็งเม็ดเลือดขาว lymphocytic เรื้อรังซึ่งการรักษาด้วยยาปฏิชีวนะไม่สามารถให้ผลลัพธ์ที่น่าพอใจ hypogammaglobulinaemia และการติดเชื้อแบคทีเรียที่เกิดขึ้นอีกในผู้ป่วยในระยะที่ราบสูงที่มี multiple myeloma ที่ไม่ตอบสนองต่อการสร้างภูมิคุ้มกันของนิวโมคอคคัส โรคเอดส์ แต่กำเนิดที่มีการติดเชื้อแบคทีเรียซ้ำ: ขนาดที่แนะนำคือ 0.2-0.4 ก. / กก. ทุกๆ 3-4 สัปดาห์ Hypogammaglobulinaemia ในผู้ป่วยหลังการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือดชนิด allogeneic ขนาดที่แนะนำคือ 0.2-0.4 กรัม / กิโลกรัมทุก 3-4 สัปดาห์ควรรักษาระดับรางน้ำให้สูงกว่า 5 กรัม / ลิตร ภาวะเกล็ดเลือดต่ำในระบบภูมิคุ้มกันขั้นต้น ตารางการรักษาทางเลือกมี 2 แบบคือ 0.8-1 ก. / กก. ในวันที่ 1; ยานี้สามารถทำซ้ำได้ 1 ครั้งภายใน 3 วันหรือ 0.4 ก. / กก. / 24 ชม. เป็นเวลา 2-5 วัน การรักษาสามารถทำซ้ำได้หากโรคกำเริบ Guillain Barre syndrome: 0.4 g / kg bw ทุกวันเป็นเวลา 5 วัน โรคคาวาซากิ: 1.6-2 ก. / กก ในปริมาณที่แบ่งเป็นเวลา 2-5 วันหรือครั้งเดียว 2 กรัม / กิโลกรัมน้ำหนักตัว ผู้ป่วยควรได้รับการรักษาด้วยกรดอะซิติลซาลิไซลิก วิธีการให้ ฉีดเข้าเส้นเลือดดำในอัตราเริ่มต้น 0.01 มล. / กก. bw / นาทีเป็นเวลา 30 นาที หากทนได้ดีอัตราการให้ยาอาจค่อยๆเพิ่มขึ้นสูงสุด 0.12 มล. / กก. / นาที
ข้อบ่งใช้
การบำบัดทดแทนในผู้ใหญ่เด็กและวัยรุ่น (0-18 ปี) กลุ่มอาการภูมิคุ้มกันบกพร่องขั้นต้นที่มีการผลิตแอนติบอดีบกพร่อง Hypogammaglobulinaemia และการติดเชื้อแบคทีเรียซ้ำในผู้ป่วยมะเร็งเม็ดเลือดขาว lymphocytic เรื้อรังซึ่งการรักษาด้วยยาปฏิชีวนะไม่สามารถให้ผลลัพธ์ที่น่าพอใจได้ Hypogammaglobulinaemia และการติดเชื้อแบคทีเรียซ้ำในผู้ป่วยที่มี multiple myeloma ในระยะที่ราบสูงที่ไม่ตอบสนองต่อการฉีดวัคซีนป้องกันโรคปอดบวม Hypogammaglobulinaemia ในผู้ป่วยหลังการปลูกถ่ายเซลล์ต้นกำเนิดเม็ดเลือดชนิด allogeneic (HSCT) โรคเอดส์ แต่กำเนิดที่มีการติดเชื้อแบคทีเรียซ้ำ การสร้างภูมิคุ้มกันในผู้ใหญ่และเด็กและวัยรุ่น (0-18 ปี) ภาวะเกล็ดเลือดต่ำในระบบภูมิคุ้มกันเบื้องต้น (ITP) ในผู้ป่วยที่มีความเสี่ยงสูงต่อการตกเลือดหรือก่อนการผ่าตัดเพื่อเพิ่มจำนวนเกล็ดเลือดในเลือด ทีม Guillain Barré โรคคาวาซากิ
ข้อห้าม
ความรู้สึกไวต่อสารออกฤทธิ์หรือสารเพิ่มปริมาณใด ๆ ความรู้สึกไวต่ออิมมูโนโกลบูลินของมนุษย์โดยเฉพาะในผู้ป่วยที่มีแอนติบอดีต่อ IgA
ข้อควรระวัง
จำเป็นต้องปฏิบัติตามคำแนะนำในการใช้ยาและปฏิบัติตามอัตราการแช่ที่กำหนดไว้อย่างเคร่งครัด ผู้ป่วยควรได้รับการตรวจสอบอย่างรอบคอบเพื่อหาผลข้างเคียงระหว่างการฉีดยา ผลข้างเคียงบางอย่างอาจพบได้บ่อยในอัตราการให้ยาสูงหรือในผู้ป่วยที่ได้รับอิมมูโนโกลบูลินปกติของมนุษย์เป็นครั้งแรกหรือในบางกรณีที่หายากเมื่อเปลี่ยนจากอิมมูโนโกลบูลินปกติของมนุษย์ไปเป็นการเตรียมการอื่นหรือหลังจากช่วงเวลาที่นานขึ้นจากช่วงเวลาของการให้ยาครั้งก่อน สามารถหลีกเลี่ยงภาวะแทรกซ้อนที่อาจเกิดขึ้นได้โดยตรวจสอบให้แน่ใจว่าผู้ป่วย: ไม่ไวต่ออิมมูโนโกลบูลินปกติของมนุษย์โดยเริ่มให้ยาในอัตราที่ช้า (0.01 ถึง 0.02 มล. / กก. / นาที) ได้รับการตรวจสอบอย่างรอบคอบสำหรับอาการใด ๆ ตลอดระยะเวลาการให้ยาโดยเฉพาะอย่างยิ่งผู้ป่วยที่ไม่เคยได้รับการรักษาด้วยอิมมูโนโกลบูลินปกติของมนุษย์ผู้ป่วยที่เคยได้รับการเตรียม IVIg ทางเลือกก่อนหน้านี้หรือหากผ่านไปนานแล้วตั้งแต่การให้ยาครั้งก่อนควรได้รับการตรวจสอบในระหว่างการให้ยาครั้งแรกและในช่วงชั่วโมงแรกหลังจากเสร็จสิ้น ควรติดตามผู้ป่วยรายอื่นทั้งหมดอย่างน้อย 20 นาที หลังการเตรียมการ หากเกิดอาการไม่พึงประสงค์อัตราการให้ยาจะต้องลดลงหรือหยุดชะงัก ในกรณีที่เกิดอาการช็อกควรเริ่มการรักษาพยาบาลที่เหมาะสม ในผู้ป่วยทุกรายการให้ Ig ทางหลอดเลือดดำต้องการ: การให้ความชุ่มชื้นอย่างเพียงพอของผู้ป่วยก่อนเริ่มการให้ยา Ig ทางหลอดเลือดดำการติดตามการขับปัสสาวะการตรวจสอบระดับครีเอตินีนในซีรัมหลีกเลี่ยงการใช้ยาขับปัสสาวะแบบลูปร่วมกัน ปฏิกิริยาภูมิไวเกินที่แท้จริงนั้นหายาก: สามารถเกิดขึ้นได้ในผู้ป่วยที่มีแอนติบอดีต่อ IgA ยานี้ไม่ได้ระบุไว้ในผู้ป่วยที่มีการขาด IgA แบบคัดเลือกซึ่งการขาด IgA เป็นความผิดปกติเพียงอย่างเดียว ในบางกรณีการให้อิมมูโนโกลบูลินของมนุษย์อาจทำให้ความดันโลหิตลดลงด้วยปฏิกิริยาแอนาฟิแล็กติกแม้ในผู้ป่วยที่เคยทนต่อการรักษาอิมมูโนโกลบูลินของมนุษย์ ควรใช้ IVIg infusions ด้วยความระมัดระวังในผู้ป่วยที่มีน้ำหนักเกินและในผู้ป่วยที่มีปัจจัยเสี่ยงต่อการเกิดลิ่มเลือดเช่นอายุมากความดันโลหิตสูงเบาหวานโรคหลอดเลือดหรือประวัติของเหตุการณ์ลิ่มเลือดอุดตันความผิดปกติของลิ่มเลือดอุดตันที่ได้มาหรือมา แต่กำเนิดการตรึงเป็นเวลานานรุนแรง ภาวะน้ำตาลในเลือดต่ำโรคที่ความหนืดของเลือดเพิ่มขึ้น มีรายงานกรณีของไตวายเฉียบพลันในผู้ป่วยที่ได้รับการเตรียม IVIg ปัจจัยเสี่ยงเช่นไตวายที่มีอยู่ก่อนเบาหวานภาวะน้ำตาลในเลือดต่ำน้ำหนักตัวเกินยาที่เป็นพิษต่อไตร่วมกันอายุมากกว่า 65 ปีได้รับการระบุในกรณีส่วนใหญ่ ในกรณีของความผิดปกติของไตควรหยุดการรักษาด้วย IVIg รายงานความผิดปกติและไตวายเฉียบพลันเกี่ยวข้องกับการใช้ผลิตภัณฑ์ IVIg ที่ได้รับการอนุมัติจำนวนมาก (ประกอบด้วยซูโครสกลูโคสมอลโตสเป็นสารเพิ่มปริมาณ) แต่การเตรียมการที่มีซูโครสเป็นตัวทำให้คงตัวมีส่วนทำให้จำนวนผู้ป่วยโดยรวมไม่ได้สัดส่วน ในผู้ป่วยที่มีความเสี่ยงอาจพิจารณาใช้ผลิตภัณฑ์ IVIg ที่ไม่มีสารเพิ่มปริมาณเหล่านี้ ในผู้ป่วยที่มีความเสี่ยงสูงต่อการเกิดไตวายเฉียบพลันหรืออาการไม่พึงประสงค์จากลิ่มเลือดอุดตันควรให้ยา IVIg ในอัตราขั้นต่ำของการให้ยาและปริมาณที่ทำได้ มีรายงานเกี่ยวกับโรคเยื่อหุ้มสมองอักเสบปลอดเชื้อ (AMS) ร่วมกับการรักษาด้วย IVIg การยุติการรักษาด้วย IVIg ส่งผลให้ AMS หายไปภายในไม่กี่วันโดยไม่มีผลสืบเนื่อง ผู้รับ IVIg ควรได้รับการตรวจติดตามอาการและอาการแสดงของเม็ดเลือดแดง แม้จะมีมาตรการมาตรฐานในการป้องกันการติดเชื้อที่แพร่กระจายด้วยการเตรียมโดยอาศัยเลือดของมนุษย์หรือพลาสมา แต่เมื่อมีการเตรียมการดังกล่าวความเป็นไปได้ในการแพร่เชื้อของเชื้อก็ไม่สามารถแยกออกได้ทั้งหมด นอกจากนี้ยังใช้กับไวรัสที่ไม่รู้จักหรืออุบัติใหม่หรือเชื้อโรคอื่น ๆ วิธีการที่ใช้ถือได้ว่ามีประสิทธิภาพในการป้องกันการแพร่กระจายของไวรัสที่ห่อหุ้มเช่น HIV, HBV และ HCV แต่อาจมีการใช้งานที่ จำกัด กับไวรัสที่ไม่ห่อหุ้มเช่น HAV และ parvovirus B19 ประสบการณ์ทางคลินิกแสดงให้เห็นว่าไม่มีไวรัสตับอักเสบเอหรือพาร์โวไวรัสบี 19 ติดต่อผ่านการเตรียมอิมมูโนโกลบูลิน นอกจากนี้ยังควรที่การมีแอนติบอดีที่มีอยู่ในการเตรียมการเหล่านี้ก่อให้เกิดความปลอดภัยของการเตรียมการเหล่านี้ มีรายงานเกี่ยวกับอาการบวมน้ำในปอดที่ไม่เป็นโรคหัวใจและหลอดเลือด (การบาดเจ็บที่ปอดหลังการถ่ายเลือดเฉียบพลัน - ความทุกข์ทางเดินหายใจอย่างรุนแรงอาการบวมน้ำในปอดภาวะออกซิเจนในเลือดต่ำการทำงานของหัวใจห้องล่างซ้ายตามปกติและมีไข้ 1-6 ชั่วโมงหลังการถ่าย) ในผู้ป่วยที่ได้รับ IVIG ควรให้ความระมัดระวังเมื่อให้ยา Octagam แม้ว่าจนถึงขณะนี้ยังไม่มีการสังเกตกรณีดังกล่าวหลังจากการให้ยานี้ ภาวะหัวใจและหลอดเลือดเกิน (ปริมาตร) อาจเกิดขึ้นได้ในระหว่างการให้ยา IVIG เมื่อปริมาณของยาเตรียมและการให้ยาอื่น ๆ ทำให้เกิดภาวะไขมันในเลือดสูงเฉียบพลันและอาการบวมน้ำในปอดเฉียบพลัน ยานี้มีโซเดียมไม่เกิน 0.03 mmol (0.69 mg) ต่อมิลลิลิตรของสารละลาย สิ่งนี้ควรนำมาพิจารณาในผู้ป่วยที่รับประทานอาหารโซเดียมควบคุม
กิจกรรมที่ไม่พึงปรารถนา
ทั่วไป: แพ้ง่ายปวดศีรษะคลื่นไส้ไข้อ่อนเพลียปฏิกิริยาในบริเวณที่ฉีด ผิดปกติ: กลาก, ปวดหลัง, หนาวสั่น, เจ็บหน้าอก หายากมาก: เม็ดเลือดขาว, โรคโลหิตจางเม็ดเลือดแดง, ภาวะช็อกจากภาวะแอนาไฟแล็กติก, ปฏิกิริยาอะนาไฟแล็กตอยด์, แองจิโออีดีมา, อาการบวมน้ำที่ใบหน้า, อาการสับสน, ความกระสับกระส่าย, ความวิตกกังวล, กล้ามเนื้อสมอง, เยื่อหุ้มสมองอักเสบปลอดเชื้อ, การสูญเสียสติ, ความผิดปกติของการพูด, ไมเกรน, เวียนศีรษะ, hypoaesthesia, paraesthesia, photophobia, การสั่นสะเทือน, ความบกพร่องทางสายตา, กล้ามเนื้อหัวใจตาย, angina, bradycardia, tachycardia, palpitations, cyanosis, thrombosis, การไหลเวียนโลหิต, ความล้มเหลวของระบบไหลเวียนโลหิตส่วนปลาย, phlebitis, ความดันเลือดต่ำ, ความดันโลหิตสูง, ซีด, เส้นเลือดอุดตันในปอด, , อาการบวมน้ำในปอด, หลอดลมหดเกร็ง, ภาวะขาดออกซิเจน, หายใจลำบาก, ไอ, อาเจียน, ท้องร่วง, ปวดท้อง, ผิวหนังลอก, ลมพิษ, ผื่น, ผื่นแดง, ผิวหนังอักเสบ, อาการคัน, ผมร่วง, ปวดกล้ามเนื้อ, ปวดปลายแขน, ปวดคอ , กล้ามเนื้อกระตุก, กล้ามเนื้ออ่อนแรง, กล้ามเนื้อและกระดูกตึง, ไตวายเฉียบพลัน, ปวดไต k, อาการบวมน้ำ, อาการคล้ายไข้หวัด, ร้อนวูบวาบ, หน้าแดง, รู้สึกเย็น, รู้สึกร้อน, เหงื่อออก, ไม่สบายตัว, รู้สึกไม่สบายหน้าอก, ความรู้สึกหงุดหงิด, ง่วงซึม, แสบร้อน, เอนไซม์ตับเพิ่มขึ้น, การทดสอบน้ำตาลในเลือดที่ผิดพลาด
การตั้งครรภ์และให้นมบุตร
การตั้งครรภ์ ความปลอดภัยของการเตรียมในหญิงตั้งครรภ์ไม่ได้รับการยอมรับในการทดลองทางคลินิกที่มีการควบคุม ควรให้ยาเตรียมกับสตรีมีครรภ์และสตรีให้นมบุตรด้วยความระมัดระวังเป็นพิเศษ การเตรียม IVIg ข้ามรกซึ่งเพิ่มขึ้นในช่วงไตรมาสที่สาม ประสบการณ์ทางคลินิกเกี่ยวกับการใช้อิมมูโนโกลบูลินบ่งชี้ว่าไม่มีผลอันตรายต่อการตั้งครรภ์พัฒนาการของทารกในครรภ์หรือทารกแรกเกิด การให้นม. อิมมูโนโกลบูลินจะหลั่งออกมาในน้ำนมแม่และอาจช่วยป้องกันทารกแรกเกิดจากเชื้อโรคที่ซึมผ่านเยื่อบุ การเจริญพันธุ์. ประสบการณ์ทางคลินิกเกี่ยวกับการใช้อิมมูโนโกลบูลินชี้ให้เห็นว่าไม่คาดว่าจะมีผลกระทบที่เป็นอันตรายต่อภาวะเจริญพันธุ์
ความคิดเห็น
ผลข้างเคียงบางอย่างอาจทำให้ความสามารถในการขับขี่และการใช้เครื่องจักรลดลง ผู้ป่วยที่มีอาการข้างเคียงระหว่างการรักษาควรรอให้อาการเหล่านี้หายไปก่อนขับรถหรือใช้เครื่องจักร หลังจากได้รับอิมมูโนโกลบูลินอาจมีการเพิ่มขึ้นชั่วคราวของระดับของแอนติบอดีที่ถ่ายโอนโดยไม่ได้รับอนุญาตในเลือดของผู้ป่วยซึ่งอาจนำไปสู่ผลบวกที่ผิดพลาดในการทดสอบทางเซรุ่มวิทยา แอนติบอดีที่ถ่ายโอนโดยไม่ใช้แอนติเจนต่อแอนติเจนของเม็ดเลือดแดงเช่น A, B, D อาจรบกวนผลการทดสอบทางเซรุ่มวิทยาเช่นการทดสอบแอนติโกลบูลินโดยตรง (การทดสอบของคูมบ์ส) ในผู้ป่วยที่ได้รับการรักษาด้วยการเตรียม IVIG อัตราการตกตะกอนของเม็ดเลือดแดง (ESR) อาจสูงขึ้นอย่างไม่ถูกต้อง (ไม่เพิ่มการอักเสบ) การเตรียมประกอบด้วยมอลโตสดังนั้นการกำหนดความเข้มข้นของกลูโคสจึงต้องดำเนินการโดยใช้วิธีการเฉพาะสำหรับกลูโคส
การโต้ตอบ
อิมมูโนโกลบูลินที่มีอยู่ในการเตรียมการอาจลดประสิทธิภาพของวัคซีนหัดคางทูมหัดเยอรมันหรืออีสุกอีใส (ควรรักษาช่วงเวลา 3 เดือนระหว่างการให้ยาและการฉีดวัคซีนในกรณีของการฉีดวัคซีนโรคหัดความอ่อนแอ) การตอบสนองของระบบภูมิคุ้มกันอาจคงอยู่ได้นานถึงหนึ่งปีจึงขอแนะนำให้ตรวจวัดแอนติบอดีหัดก่อนการฉีดวัคซีน) ไม่ควรผสมกับยาอื่น ๆ
สารเตรียมประกอบด้วยสารอิมมูโนโกลบูลินของมนุษย์ปกติ
ยาที่ได้รับการชดใช้: NO