พุธ 24 กรกฎาคม, 2013 - เป็นไปได้ที่จะพัฒนาวิธีการที่ง่ายและมีประสิทธิภาพมากขึ้นในการแทรกยีนเข้าไปในเซลล์ตาซึ่งสามารถขยายการรักษาด้วยยีนอย่างมีนัยสำคัญเพื่อช่วยฟื้นฟูการมองเห็นให้กับผู้ป่วยด้วยโรคบางอย่างที่ทำให้ตาบอด เช่น retinitis pigmentosa และโรคชราเช่น macular degeneration
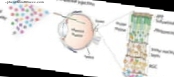
ขั้นตอนใหม่นั้นรวดเร็วและไม่ต้องผ่าตัดโดยไม่ต้องผ่าตัด ประกอบด้วยการขนส่งของยีนปกติผ่านเรตินาทั้งหมดเพื่อส่งไปยังเซลล์ที่เข้าถึงได้ยาก
ในช่วงหกปีที่ผ่านมานักวิทยาศาสตร์หลายกลุ่มประสบความสำเร็จในการรักษาผู้ป่วยโรคตาที่สืบทอดยากโดยการฉีดไวรัสที่มียีนปกติเข้าสู่เรตินาของตาด้วยยีนที่บกพร่อง . อย่างไรก็ตามแม้จะมีความจริงที่ว่ากระบวนการที่รุกรานอย่างนี้สามารถเชิญเราให้คิดว่ามันเป็นเรื่องที่รวดเร็วมาก แต่ไวรัสที่มียีนปกติไม่สามารถไปถึงเซลล์เรตินาทั้งหมดที่จำเป็นต้องได้รับการซ่อมแซม
การตอกเข็มผ่านเรตินาและฉีดไวรัสการออกแบบด้านหลังเป็นขั้นตอนการผ่าตัดที่ค่อนข้างอันตราย อย่างไรก็ตามแพทย์ไม่มีทางเลือกอื่นเนื่องจากไม่มีไวรัสที่ใช้ในการขนส่งยีนและการส่งมอบสามารถผ่านตาทั้งหมดจนกว่าจะถึงเซลล์รับแสงเซลล์ไวต่อแสงที่ยีนบำบัดต้องการ
หลังจากการวิจัย 14 ปีทีม David Schaffer ศาสตราจารย์วิศวกรรมเคมีและชีวโมเลกุลที่มหาวิทยาลัยแคลิฟอร์เนียที่ Berkeley และผู้อำนวยการศูนย์เซลล์ต้นกำเนิด Berkeley ที่ติดอยู่กับมหาวิทยาลัยนั้นได้รับไวรัสที่ถูกฉีดยาด้วยการยักย้ายถ่ายเททางพันธุกรรม ภายในอารมณ์ขันน้ำเลี้ยงตาเท่านั้นและจะนำยีนไปสู่ประชากรของเซลล์ที่เข้าถึงได้ยากด้วยวิธีที่ปลอดภัยและไม่ต้องผ่าตัดโดยไม่ต้องผ่าตัด
ไวรัสตัวใหม่นั้นทำงานได้ดีกว่าการรักษาในปัจจุบันในรูปแบบของโรคตาเสื่อมของมนุษย์สองตัวในสัตว์ฟันแทะและสามารถเจาะเซลล์รับแสงของดวงตาลิงซึ่งค่อนข้างคล้ายกับของมนุษย์
Schaffer และทีมของเขากำลังร่วมมือกับแพทย์เพื่อระบุผู้ป่วยที่จะได้รับประโยชน์มากที่สุดจากการใช้เทคนิคการป้อนยีนนี้และหลังจากการพัฒนาพรีคลินิกที่เหมาะสมคาดว่าจะไปทดลองทางคลินิก การทำงานของการปล่อยไวรัสที่มียีนนั้นไม่ต้องใช้เวลานานกว่า 15 นาทีดังนั้นจึงเป็นไปได้ว่าเมื่อเทคนิคนี้ได้รับการตรวจสอบอย่างถูกต้องผู้ป่วยที่ผ่านขั้นตอนนี้สามารถกลับบ้านได้ในวันเดียวกัน
John Flannery, Leah C. Byrne, Ryan R. Klimczak และ Meike Visel จาก University of California Berkeley รวมถึง Lu Yin และ William H. Merigan จาก University of Rochester ในนิวยอร์กก็มีส่วนร่วมในงานวิจัยและพัฒนาด้วยเช่นกัน York ทั้งสองหน่วยงานในสหรัฐอเมริกาและ Deniz Dalkara ซึ่งตอนนี้อยู่ที่สถาบันวิชั่นในปารีสประเทศฝรั่งเศส
ที่มา:
แท็ก:
อาหารการกิน ต่าง เพศ
ขั้นตอนใหม่นั้นรวดเร็วและไม่ต้องผ่าตัดโดยไม่ต้องผ่าตัด ประกอบด้วยการขนส่งของยีนปกติผ่านเรตินาทั้งหมดเพื่อส่งไปยังเซลล์ที่เข้าถึงได้ยาก
ในช่วงหกปีที่ผ่านมานักวิทยาศาสตร์หลายกลุ่มประสบความสำเร็จในการรักษาผู้ป่วยโรคตาที่สืบทอดยากโดยการฉีดไวรัสที่มียีนปกติเข้าสู่เรตินาของตาด้วยยีนที่บกพร่อง . อย่างไรก็ตามแม้จะมีความจริงที่ว่ากระบวนการที่รุกรานอย่างนี้สามารถเชิญเราให้คิดว่ามันเป็นเรื่องที่รวดเร็วมาก แต่ไวรัสที่มียีนปกติไม่สามารถไปถึงเซลล์เรตินาทั้งหมดที่จำเป็นต้องได้รับการซ่อมแซม
การตอกเข็มผ่านเรตินาและฉีดไวรัสการออกแบบด้านหลังเป็นขั้นตอนการผ่าตัดที่ค่อนข้างอันตราย อย่างไรก็ตามแพทย์ไม่มีทางเลือกอื่นเนื่องจากไม่มีไวรัสที่ใช้ในการขนส่งยีนและการส่งมอบสามารถผ่านตาทั้งหมดจนกว่าจะถึงเซลล์รับแสงเซลล์ไวต่อแสงที่ยีนบำบัดต้องการ
หลังจากการวิจัย 14 ปีทีม David Schaffer ศาสตราจารย์วิศวกรรมเคมีและชีวโมเลกุลที่มหาวิทยาลัยแคลิฟอร์เนียที่ Berkeley และผู้อำนวยการศูนย์เซลล์ต้นกำเนิด Berkeley ที่ติดอยู่กับมหาวิทยาลัยนั้นได้รับไวรัสที่ถูกฉีดยาด้วยการยักย้ายถ่ายเททางพันธุกรรม ภายในอารมณ์ขันน้ำเลี้ยงตาเท่านั้นและจะนำยีนไปสู่ประชากรของเซลล์ที่เข้าถึงได้ยากด้วยวิธีที่ปลอดภัยและไม่ต้องผ่าตัดโดยไม่ต้องผ่าตัด
ไวรัสตัวใหม่นั้นทำงานได้ดีกว่าการรักษาในปัจจุบันในรูปแบบของโรคตาเสื่อมของมนุษย์สองตัวในสัตว์ฟันแทะและสามารถเจาะเซลล์รับแสงของดวงตาลิงซึ่งค่อนข้างคล้ายกับของมนุษย์
Schaffer และทีมของเขากำลังร่วมมือกับแพทย์เพื่อระบุผู้ป่วยที่จะได้รับประโยชน์มากที่สุดจากการใช้เทคนิคการป้อนยีนนี้และหลังจากการพัฒนาพรีคลินิกที่เหมาะสมคาดว่าจะไปทดลองทางคลินิก การทำงานของการปล่อยไวรัสที่มียีนนั้นไม่ต้องใช้เวลานานกว่า 15 นาทีดังนั้นจึงเป็นไปได้ว่าเมื่อเทคนิคนี้ได้รับการตรวจสอบอย่างถูกต้องผู้ป่วยที่ผ่านขั้นตอนนี้สามารถกลับบ้านได้ในวันเดียวกัน
John Flannery, Leah C. Byrne, Ryan R. Klimczak และ Meike Visel จาก University of California Berkeley รวมถึง Lu Yin และ William H. Merigan จาก University of Rochester ในนิวยอร์กก็มีส่วนร่วมในงานวิจัยและพัฒนาด้วยเช่นกัน York ทั้งสองหน่วยงานในสหรัฐอเมริกาและ Deniz Dalkara ซึ่งตอนนี้อยู่ที่สถาบันวิชั่นในปารีสประเทศฝรั่งเศส
ที่มา: